Ernest Rutherford
[1871-1937] Nació en Nueva Zelanda, donde cursó sus estudios superiores graduándose en física y matemática. En 1895 viaja a Cambridge, Inglaterra, para trabajar en el laboratorio Cavendish[1] bajo la dirección de J. J. Thomson y comienza a estudiar los recientemente descubiertos rayos X.
También estudia la radiación descubierta por Becquerel en el uranio y encuentra dos clases de rayos a los que llama alfa y beta. Los primeros son partículas con carga positiva que no pueden penetrar facilmente en la materia, mientras que los segundos, que si lo hacen, resultan ser electrones.
En 1898 viaja a Montreal, Canadá, donde permanece 9 años. Durante esa etapa, conjuntamente con Frederick Soddy (premio Nobel de Química en 1921) obtienen las leyes de las desintegraciones radiactivas y descubren que la radioactividad es un proceso mediante el cual los átomos de un elemento se convierten en átomos de otro elemento diferente. Rutherford adquiere tal prestigio que se le otorga el cargo de jefe del departamento de Física en la Universidad de Manchester, Inglaterra. Allí trabaja por más de diez años generando un centro de investigación en radioactividad de renombre internacional. En 1908 es galardonado con el premio Nobel de Química . En esa época colabora con Geiger y Marsden, con quienes diseña y realiza un experimento que fue crucial en la historia de la física. Cuando bombardeaban láminas de oro con partículas alfa vieron que algunas de ellas eran desviadas con respecto a la dirección de incidencia en más de 90 grados, (como si la partícula alfa rebotara contra la lámina). Este resultado entraba en contradicción con el modelo del átomo de Thomson indicando que la distribución de carga en el átomo sería distinta a la supuesta.
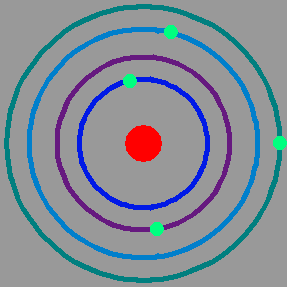
En el año 1911 Rutherford postula un modelo revolucionario del átomo al que describe como si fuera un sistema solar en miniatura, donde el núcleo cargado positivamente ocupaba una muy pequeña fracción del volumen total del átomo, representaba al sol, y los electrones a su alredor a los planetas. Este modelo explicaba satisfactoriamente los rebotes detectados al chocar las partículas alfa contra las láminas de oro, las partículas alfa rebotaban al chocar con los núcleos.
Tamaño del núcleo: El radio atómico en el caso del átomo de oro es 18.000 veces mayor que el tamaño del núcleo. Si lo comparecemos con el sistema solar, en una escala en la que el sol y el núcleo fueran del mismo tamaño, esto significaría que el electrón más externo, o sea el que está más lejos del núcleo, dista de este el doble de la distancia que hay entre Plutón y el Sol!! Esto contrasta con el hecho de que en un espacio tan pequeño el núcleo concentra la mayor parte de la masa del átomo.
Rutherford postula más tarde la existencia del neutrón (partícula sin carga). En 1919, Rutherford sucede a Thomson en la dirección del laboratorio Cavendish, cargo que ocupa hasta 1937. Durante esa época, realiza una serie de experiencias por las cuales al bombardear átomos de un elemento con partículas alfa se producen átomos de otro elemento y al mismo tiempo en cada uno de los procesos es emitido un núcleo de Hidrógeno. Como resultado de estos experimentos resultó evidente el papel fundamental de dichos núcleos en la estructura atómica, comprobándose también que la carga positiva de cualquier núcleo podía obtenerse como un número entero de veces la del núcleo de Hidrógeno. Había hecho su aparición en escena el protón y ya para fines de 1920 los núcleos de Hidrógeno se denominaban regularmente protones.
Debug data: